口服耐受是肠道黏膜免疫系统识别食物、共生菌等无害抗原、避免免疫系统过度激活、从而维持肠道稳态的重要机制。近年来,表达转录因子RORγt的抗原提呈细胞(RORγt⁺ APCs),包括3型天然淋巴样细胞(ILC3s)和Thetis细胞等,被发现通过诱导抗原特异性调节性T细胞(Treg)在口服耐受和肠道稳态维持中发挥关键作用,然而其具体调控机制仍不清楚。
RORγt是调控ILC3s和Th17细胞分化的谱系决定转录因子,其在两类细胞中的调控机制存在显著差异。尽管Rorc基因座上已有多个顺式调控元件(如CNS6、CNS9和RORCE2等)被报道参与T细胞中RORγt的表达调控,但在ILC3s中特异性调控RORγt表达的元件至今尚未明确。
因此,鉴定调控RORγt⁺ APC中RORγt表达的特异性顺式调控元件,阐明其在食物及菌群抗原特异性Treg诱导中的作用,对于深入理解口服耐受的建立机制、探索过敏与炎症性疾病的新干预策略具有重要意义。

近日,清华大学基础医学院郭晓欢课题组在《Nature Communications》在线发表题为“RORγt⁺ APCs require a distinct cis-regulatory element to instruct tolerance to dietary antigens”的研究论文。该研究首次鉴定出一个特异性调控RORγt⁺ APCs的顺式调控元件OCR369,揭示了其通过招募RUNX3及介导染色质环形成等机制,维持ILC3s等RORγt⁺天然免疫细胞中RORγt的表达,进而调控食物抗原特异性Treg分化及口服耐受建立。该发现不仅阐明了RORγt在RORγt⁺ APCs中与T细胞不同的调控模式,也为理解其在肠道免疫耐受中的功能提供了新视角。
研究人员首先通过ATAC-seq分析发现,位于Rorc基因内含子区的开放染色质区域OCR369在ILC3s中具有较高的染色质可及性,而在Th17和RORγt⁺ Treg等适应性免疫细胞中较低,该特征在人类ILC3s中也高度保守。为进一步解析其功能,团队利用CRISPR-Cas9技术构建了OCR369敲除小鼠(RorcΔ369)。结果显示,OCR369缺失特异性地导致肠道ILC3s数量减少、RORγt表达下降,以及IL-17A和IL-22等效应分子水平降低,而对Th17和RORγt⁺ Treg细胞无显著影响。骨髓嵌合体和体外ILC分化实验进一步证实,OCR369对ILC3的发育与RORγt表达具有内在调控作用。结合单细胞ATAC-seq数据分析,OCR369在RORγt⁺ APC各亚群中亦表现出不同程度的开放状态。单细胞测序与光谱流式分析进一步揭示,在断奶期(3周龄),OCR369主要调控RORγt⁺ DC样细胞;而在成年期(6周龄),其对MHCII⁺ ILC3s和RORγt⁺ DC样细胞均发挥关键调控作用。
机制研究表明,OCR369通过招募转录因子RUNX3并形成染色质环与Rorc启动子相互作用,增强ILC3s中RORγt的表达。RUNX3在ILC3s及RORγt⁺ APCs中高表达,DNA pull-down联合质谱分析鉴定其为OCR369关键结合蛋白,CUT&RUN实验进一步证实其在ILC3s中特异性结合OCR369位点,且该结合在OCR369缺失后显著减弱。3C-qPCR实验亦证实OCR369与Rorc启动子之间存在特异性染色质环相互作用。
功能层面,OCR369缺失小鼠随年龄增长出现自发性小肠炎症,表现为小肠长度增加、绒毛延长、杯状细胞与簇细胞增生、肥大细胞浸润及细胞外基质沉积,伴随RORγt⁺ Treg减少、Th2/Th17细胞及相关细胞因子上调。进一步通过H. hepaticus定植模型与OVA口服耐受模型发现,OCR369依赖的RORγt⁺ APCs在诱导微生物及食物抗原特异性RORγt⁺ Treg分化、建立口服耐受中发挥核心作用。OCR369缺失导致抗原特异性Treg诱导失败,反而促进Th2和Th17型炎症反应。体外共培养实验亦证实,OCR369缺失的RORγt⁺ APCs诱导Treg分化的能力显著受损。在OVA诱导的迟发型超敏反应耐受模型中,OCR369缺失小鼠不仅丧失耐受建立能力,反而加剧了食物抗原特异性炎症反应。这进一步强调了OCR369依赖的RORγt⁺ APCs在维持口服耐受中的关键作用。
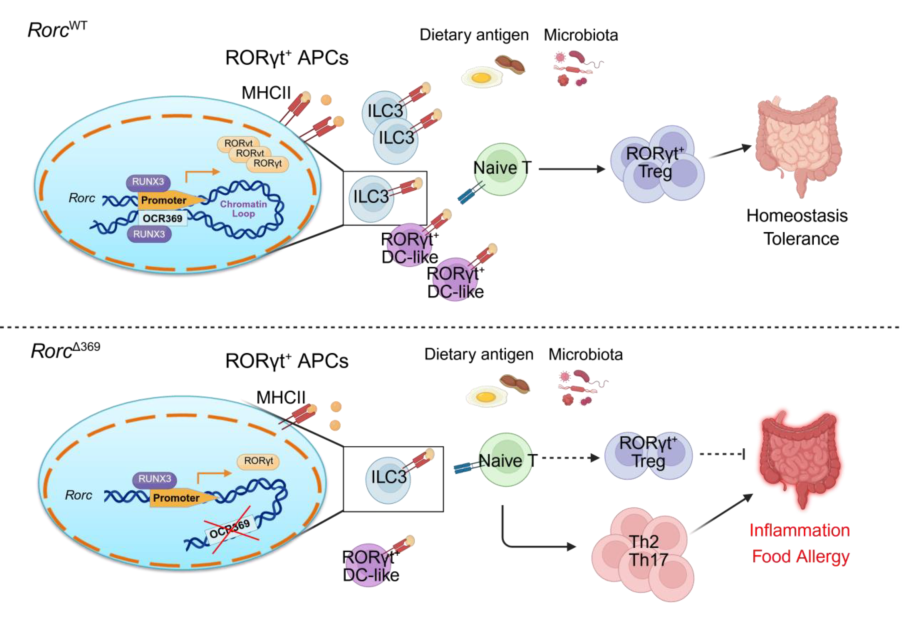
OCR369通过调控RORγt⁺抗原提呈细胞维持肠道免疫耐受
综上,本研究首次鉴定出特异性调控RORγt⁺ APCs的顺式调控元件OCR369,阐明了其通过RUNX3结合与染色质环形成维持RORγt高表达的分子机制,并揭示了其在协同调控食物与微生物抗原耐受、维持肠道稳态中的关键作用。研究还提出了RORγt⁺ APC亚群在生命不同阶段功能分工的新模型,强调了其协同维持食物耐受的动态调控机制。OCR369的发现不仅加深了对ILC3与T细胞RORγt调控机制差异的理解,也为靶向RORγt⁺ APCs治疗食物过敏和炎症性肠病等疾病提供了新靶点。
清华大学基础医学院副教授郭晓欢为本文通讯作者。清华大学已毕业博士生赵杰、博士后郝嘉成、博士生陈金诚为共同第一作者。研究得到康奈尔大学Gregory F. Sonnenberg教授、清华大学朱可可教授等多方合作支持,并获得国家自然科学基金、国家重点研发计划、北京市自然科学基金、生物制药制备与递送国家重点实验室开放课题及拜耳研究者奖等项目资助。郭晓欢课题组长期聚焦肠道黏膜免疫与菌群稳态调控研究,近年来在Nat Microbiol、J Exp Med、Sci Immunol、Cell Metab、Nat Commun等期刊发表系列重要成果,揭示了ILC3s等黏膜免疫细胞在维持黏膜稳态与控制黏膜疾病如感染、炎症、肿瘤等中发挥的关键作用与新机制。
原文链接:
https://www.nature.com/articles/s41467-026-69886-z.